
第65期
出刊日:2023-07-15
返回上一層乳癌威脅日增, 治療有突破!
乳癌是女性頭號大敵,尤其台灣好發年齡早歐美10年,更需從年輕開始關心乳房健康。所幸近年針對HER2陽性乳癌與惡性度高的三陰性乳癌,新藥有所突破,新型ADC抗體藥物複合體提供精準治療,有助於提升存活率!
諮詢/王明暘(臺大醫院外科部主治醫師、臺大醫學院外科臨床副教授)
撰稿/林貞岑
35歲的美芳得知確診乳癌時,當下心碎、眼淚潰堤,多年來持續做不孕症治療的她,多麽期待寶寶降臨,如今卻可能再也沒有機會一圓為人母心願。不過,回診時醫師捎來讓她振奮的好消息,乳癌的療法愈來愈多,療效愈來愈好,還是有機會生育下一代。

乳癌是台灣女性好發癌症首位,2020年有15259人罹病,相當於每天有41人被診斷罹患乳癌;2022年則有2834人因乳癌喪命,居女性十大癌症死因第三位,相當於每天有7人因此失去寶貴性命。
台灣乳癌病人罹癌時間平均較歐美提早10年,有7成乳癌患者是在40~69歲這個年齡區間,而近年來40歲以下就罹患乳癌的名人也不在少數,因名人效應讓人心驚,像聲音嘹亮的歌手朱俐靜、阿桑,離世時還不到40歲;以「犀利人妻」獲得金鐘獎最佳女配角的朱芯儀,36歲確診乳癌時已轉移到淋巴,經過手術及藥物治療後狀況穩定,近期宣布戰勝病魔,甚至出書細數抗癌的心路歷程,她樂觀積極勇敢的抗癌經驗,鼓勵了許多人。
乳癌發生率逐年攀升,且對年輕女性威脅日增,幸而新藥發展快速,治療方法也愈來愈多元。現在早期乳癌幾乎可以治癒,即使轉移性的晚期乳癌,也有機會好好控制,存活率大增,愈來愈趨近慢性病治療。
乳癌依病理指標分4型 邁向精準、個人化治療
隨著人類基因體解碼,不少形成乳癌的機轉及路徑已能被掌控,個人化精準治療時代正式來臨。
針對不同基因特性、善用多種藥物精準抑癌,是乳癌治療新趨勢。以往僅能用化學療法(如紫杉醇)、抗荷爾蒙藥物(如泰莫西芬)及標靶藥物來延緩疾病惡化,如今加入免疫療法等多種新藥靈活搭配,更能準確殺滅癌細胞、維持生活品質。
一旦診斷出乳癌,會根據以下4個病理指標來判斷是哪一種型別:
1 第二型人類表皮生長因子受體(HER2)
2 荷爾蒙類的動情素受體(Estrogen Receptor, ER)
3 黃體素接受體(Progesterone receptor, PR)
4 細胞生長分裂指數(Ki-67)
從上述病理指標的陽性、陰性以及數據高低,可概分為4種亞型:管腔A型、管腔B型、HER2陽性及三陰性乳癌。台灣以管腔型乳癌居多,占6到7成。每一型的臨床特徵、預後及治療策略各不相同,因此衍生出個人化治療(見下頁表),也有許多值得期待的新藥。
標靶、免疫療法新藥輩出
例如,目前針對管腔型乳癌的新藥標靶藥物為CDK4/6抑制劑,是可直接抑制癌細胞分裂週期的重要蛋白質,療效佳,相較化療來說副作用更小,不僅可以延長存活時間,並可延後患者接受化療的時間,甚至可延後達4年以上,已被國際列為治療準則。健保署於2019年通過用於管腔型乳癌治療。
至於過去無藥可用的轉移性、晚期乳癌,或是難治療的三陰性乳癌,如今免疫療法與標靶新藥出現,皆突破了困境。
免疫療法是透過活化病人本身的免疫系統,讓免疫細胞發揮功能、攻擊癌細胞。癌細胞相當狡詐,會結合特定的生物標記如PD-1、 PD-L1等表面蛋白把自己隱藏起來,躲過免疫T細胞的檢核機制,讓它誤把敵人當朋友,不去攻擊癌細胞。免疫療法利用單株抗體與癌細胞的PD-L1結合,揭開癌細胞偽裝,讓自身的免疫系統集中火力擊殺腫瘤。
2019年美國食品藥物管理署(FDA)核可第一個使用在轉移性三陰性乳癌患者的免疫治療藥物癌自禦(Atezolizumab),研究結果發現,該藥合併標準化療,有70%的PD-L1陽性患者得到明顯效果,即使PD-L1陰性患者,也有30%的治療率,甚至有10%的轉移性乳癌患者追蹤5年仍沒有復發跡象。
另項針對1174位患者的研究指出,高風險早期三陰性乳癌,術前以免疫療法搭配化療,有機會提升「病理完全反應」(pathological complete response, pCR),意指沒有發現殘留癌細胞於乳腺、淋巴腺或淋巴血管中,表示預後較好。此外,有超過6成腫瘤組織會完全消失,可以減少手術切除範圍。手術後接續免疫療法半年,可以消滅術後殘存的癌細胞,提升存活率,同時降低三成遠端惡化及復發風險。
不過,免疫療法也有風險,可能會連正常組織也遭到免疫系統攻擊,譬如攻擊腸胃道造成腹痛、拉肚子,攻擊甲狀腺造成甲狀腺低下,攻擊肌肉造成肌肉發炎、疼痛無力等,通常可以處理,不過嚴重時可能造成心律不整、心肌炎或腦膜炎,甚至喪命。
免疫療法屬於後線治療,腫瘤大於3~4公分、有淋巴結轉移,可考慮免疫療法。國內核准吉舒達(Keytruda)使用於治療三陰性乳癌,每3週打1次,需施打1年,整個療程約需兩百萬元左右,目前無健保給付。

新型ADC「魔術子彈」藥物 殺癌精準、傷害小
乳癌分類為HER2陽性者,也就是HER2基因過度表現,目前有多種標靶藥物可控制,不過這類病人不僅癌細胞生長快速,對於部分藥物也容易產生抗藥性,即使完成手術等治療,也有較高機會轉移或復發。
至於HER2陰性者,過去不適用標靶藥物,無有效藥物可治療,但近期研究發現,有部分HER2陰性的患者不完全屬於陰性,重新歸屬為「弱陽性」(HER2 low),這些人如今有新的「抗體藥物複合體」(Antibody Drug Conjugate, ADC)藥物可選擇,且此藥不管HER2表現的強弱都可以使用,也可能是一些晚期轉移患者的曙光。
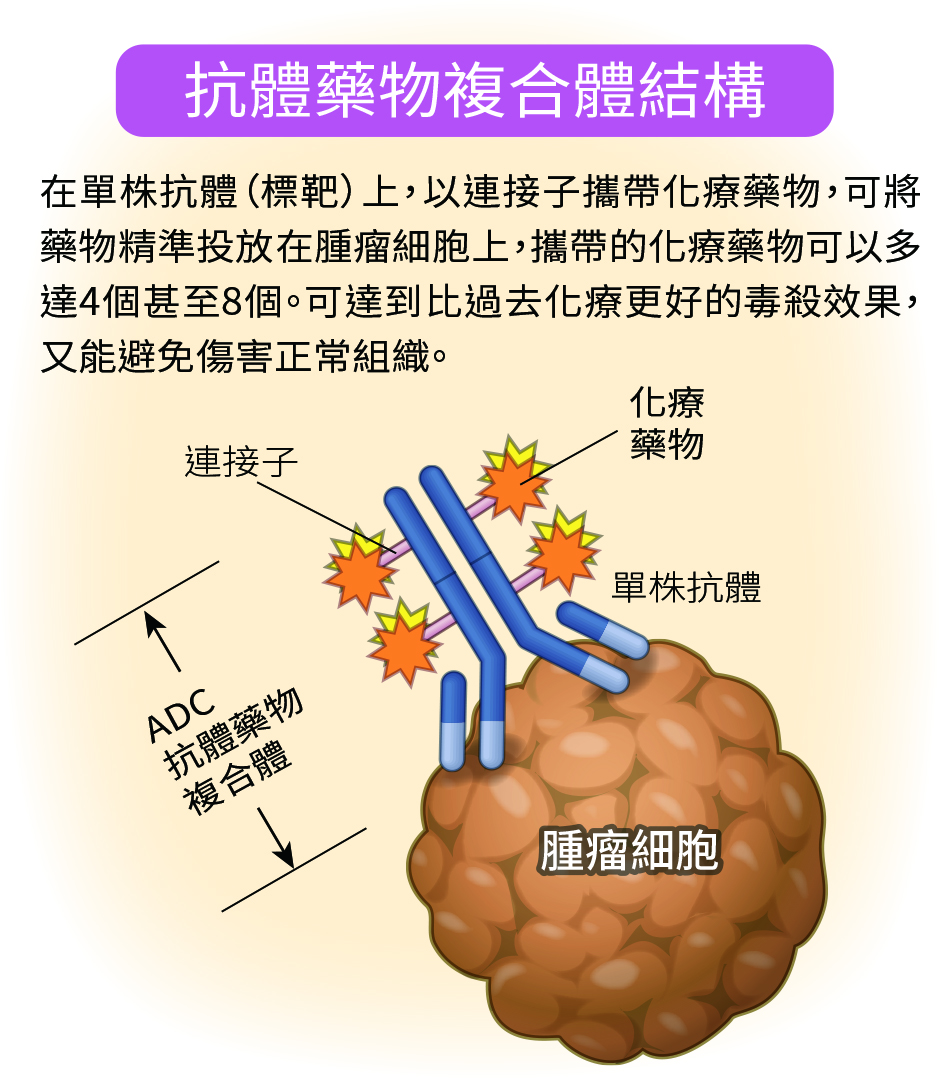
ADC又被稱為生物導彈、魔術子彈,可簡單想成是「標靶加化療」的新型藥物,原理是在單株抗體上加上連接子(linker)以攜帶化療藥物。若以弓箭比擬標靶藥物,ADC就是自帶鏡頭導航、後面綁著炸藥(化療藥)的弓箭,能瞄準切中靶心、精準毒殺癌細胞,避免波及傷害正常組織。TDM1(trastuzumab emtansine)是最早可應用於HER2陽性的ADC藥物。
新一代的ADC藥物如ENHERTU(trastuzumab deruxtecan),可承載更多化療藥物,並有較佳的細胞通透性,能穿透腫瘤細胞膜,產生旁觀者(bystander effect)效應,毒殺鄰近抗原表現不一癌細胞、除惡務盡。副作用是可能產生肺炎、胃痛及噁心嘔吐。
跟傳統化療相比,ADC藥物目標專一,它所攜帶的化療藥物毒性雖強,可是因爲精準投放,藥量少就能達到比化療更好的毒殺效果。研究證實,ADC讓轉移性HER2存活期延長近兩年半,對HER2弱陽性患者也具有療效。
2022年,美國FDA擴大ENHERTU適用範圍,先前接受標靶治療無效的HER2陽性病人,以及癌症擴散無法經由手術治療,或早期乳癌手術前或後接受抗HER2標靶治療,並在治療後6個月復發的人等都可使用,期盼ADC能成為救命的利器。國內目前也有此藥,多用在第四期乳癌的病人,需自費。
三陰性乳癌也有新款ADC藥物Sacituzumab Govitecan-hziy,是一種標靶為Trop-2的ADC藥物,在晚期三陰性乳癌具有卓越的臨床效果。Trop-2蛋白經常在許多腫瘤細胞表面過度表現,特別在三陰性乳癌細胞中,常有Trop-2蛋白高度表現,可做為重要的標靶。根據成功的臨床試驗,疾病惡化風險降低59%,死亡風險降低了52%,具有顯著療效,為長期缺乏有效療法、預後差的三陰性乳癌病患帶來新的治療武器,寫下新的三陰性乳癌治療里程碑。
三陰性乳癌突破瓶頸 治療更多元
三陰性乳癌是指腫瘤細胞上的3種受體都沒有表現。這類乳癌佔所有乳癌的15%,在台灣一年可以新增2000名患者。
晚期三陰性乳癌治療難度較高,可用藥物少、復發率高,其中以40歲以下及60歲以上的族群,復發率最高,且復發後存活期平均不到2年。
三陰性乳癌以往並無荷爾蒙及有效的標靶藥物治療,化療藥物如小紅莓、紫杉醇或鉑金類藥物是主要的選擇,現在則多了免疫製劑及ADC等藥物。
現在的三陰性乳癌治療,主要是在手術前進行「先導性化療」,好處是癌瘤縮小了,且能明顯看到腫瘤反應,做為後續用藥或改藥依據,手術切除範圍也變少,原本需要乳房全部切除的病人,也能夠留住乳房。治療過程中,會檢驗病理完全反應(pCR),如果出現pCR,表示預後良好。免疫製劑引入後,如果前導性化療合併使用,開刀時達到全病理反應,則開刀後不需再打化療,僅需進行免疫治療,如果仍有殘存腫瘤,則可再接受半年口服化學治療藥物,改善治療效果,整體存活率較過往提升許多。
此外,乳癌病患如果懷疑家族有基因突變,則可進行基因檢測,看看是否有BRCA1與BRCA2遺傳性乳癌基因等,若有,治療時可使用PARP抑制劑,在早期及晚期乳癌均有提升存活率之療效。
年輕女性罹患乳癌 可尋求保全生育方法
此外,台灣的乳癌發生年齡多好發在停經前的女性,且與40年前相比,發生率增加許多。根據衛福部國健署台灣癌症登記中心統計,40~44歲乳癌每10萬人口發生率從1980年代的33.96人,到2020年的148.36人 、45~49歲每10萬人口發生率也從42.41人上升到231.76人。
歐美的年輕乳癌患者以三陰性及侵襲性的乳癌為主,復發、死亡率高,台灣的年輕乳癌患者,以臺大醫院為例,以管腔B型偏多,相較難纏的三陰性乳癌,治療效果及存活率較好。
許多人以為,愈年輕罹患乳癌,癌細胞愈「兇險」,愈難治療?其實未必,只要及早發現,好好治療,與中老年乳癌的結果不會差太多。最怕的是年輕女性輕忽、延誤病情,或者不想治療,擔心影響外觀、工作或生育。事實上,若有乳房重建、凍卵等需求,都能與醫療團隊討論找到解決方法。
一般狀況下,若是荷爾蒙受體陽性的病人,治療後都需要吃抗荷爾蒙藥物,通常建議吃5~10年,若想懷孕生子,可由醫師依據個人狀況評估,可能先吃2~3年後停藥,生完繼續吃,目前研究顯示,因生產停藥,不影響復發率與預後。
30歲以下的患者,治療結束後大部分卵巢功能就能恢復,仍可自然懷孕,經婦產科醫師評估後,不一定得凍卵;但如果接近40歲,因治療後需要使用荷爾蒙藥物,會停經兩、三年,要再懷孕很困難,這時就要考慮先凍卵再治療,或者在醫師評估安全狀況下,停用荷爾蒙藥物備孕。
懷孕時發現乳癌 也能順利生產
一般建議懷孕3個月後,再做乳癌治療,對胎兒較安全。若剛懷孕就發現罹患乳癌,可與醫師討論是否中止妊娠,但若懷孕超過3個月,不一定都需要拿掉小孩。例如臺大醫院曾收治3位乳癌孕婦,兩位懷孕30週以上,照樣可以開刀做治療,另外一位則是懷孕6週,腫瘤較小,手術切除後不須做化療,最後均順利生下寶寶。
懷孕期間有些治療確實不能做,如放射線療法、標靶治療及抗荷爾蒙藥物。至於化療是相對安全的,但生產前最好先暫停,因為剛做完化療,白血球較低、最怕感染,而生產時會有傷口,很容易加重感染風險。
至於在使用抗荷爾蒙治療期間懷孕,則必須中斷停藥,目前研究指出,停藥生小孩的病人,乳癌復發機率並沒有比較高,因此生完小孩再繼續服藥就好。若治療已經結束才發現懷孕,就如同一般懷孕,不需要特別擔心。
整體而言,乳癌的治療已有大幅度進展,期待未來能解密更多乳癌機轉,找出阻斷不同路徑的新藥,讓乳癌不再成為女性生命的威脅!
Q停經後就不會得到乳癌?
A 錯。乳癌受女性荷爾蒙影響是長期的,荷爾蒙暴露的時間愈長,日後得到乳癌機率越高,即使停經也不會減少乳癌發生機率。歐美婦女70~80歲反而是乳癌發生高峰期,表示在早在停經前,乳房病變已經發生。所以停經後婦女,還是要定期做乳房篩檢。
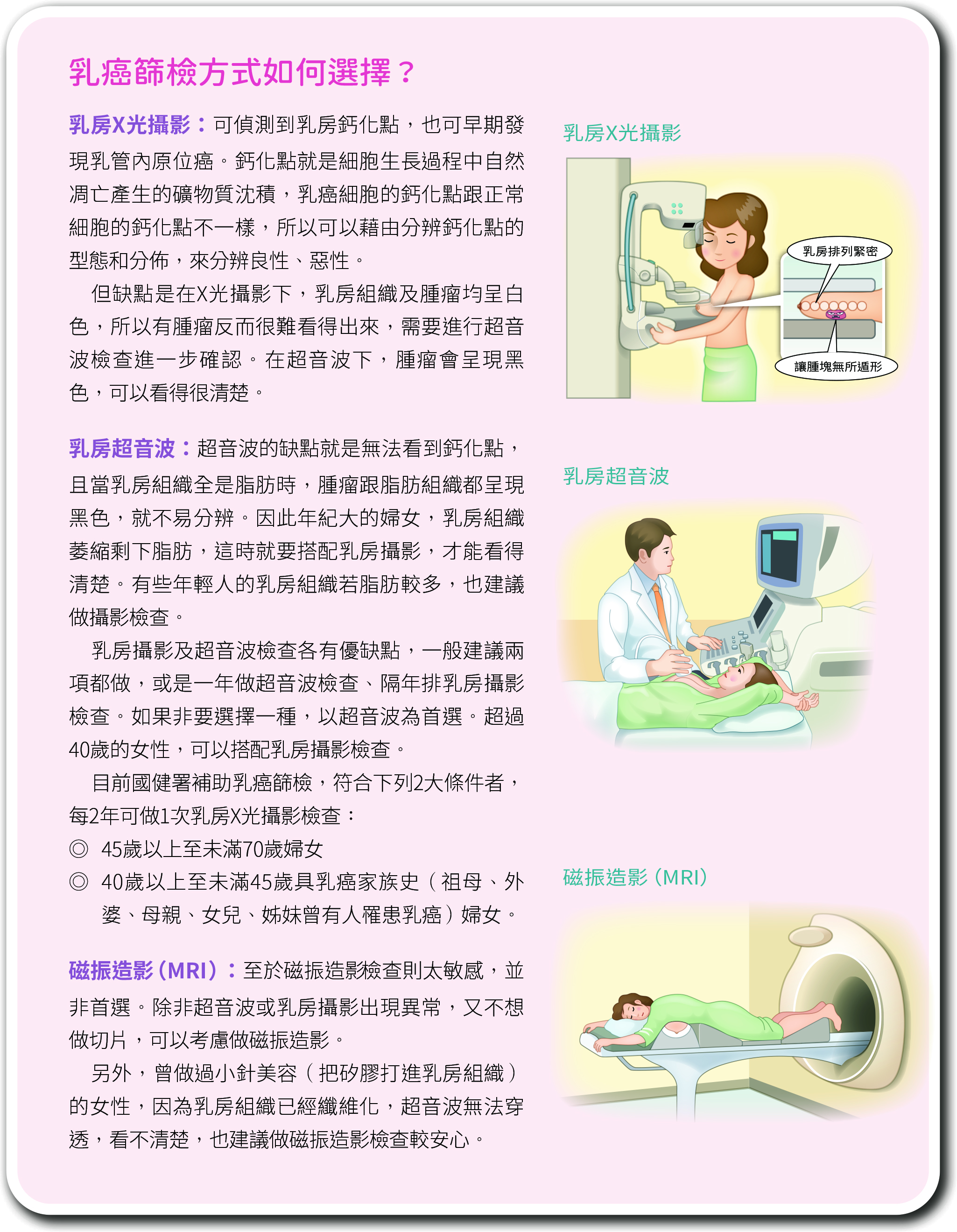
Q我的乳房組織有鈣化點,是不是不好的東西?
A許多女性一聽到乳房有鈣化點就很緊張,其實鈣化點無所謂好壞,它是組織細胞生長過程中,自然凋亡產生的礦物質沈積,就好像石頭一樣,反倒是旁邊是什麼組織造成鈣化點比較重要。而乳癌因為癌細胞生長速度較快,因此可能有鈣化點沉積在腫瘤內,這時就要做切片,辨別究竟是老化造成的普通鈣化,還是乳癌腫瘤造成的鈣化點。
Q乳房重建會影響癌症存活率?
A乳房重建是個人選擇,並不會影響乳癌的治療及存活率。現在治療趨勢是,先採取輔助化療將癌瘤縮小,再以手術切除,盡量保留乳房的外觀形狀。也可以選擇全切除再加重建,用果凍矽膠或自體組織(取最多肉的大腿、腹部、闊背肌作為皮瓣)重建乳房,可以跟醫療團隊討論出最適合自己的做法。
Q如何降低罹患乳癌風險?
A造成乳癌的風險因子太多,很難說做某件事就能遠離乳癌,目前最多研究證實的是:天天五蔬果,增加蔬菜水果攝取量,可以預防包括乳癌在內的所有癌症。
請別錯過本期其他精彩內容…
- 編輯筆記 / 「魔術子彈」助攻 乳癌治療新突破
- 新聞NEWS一下 / 2022年國人十大死因 新冠肺炎高居第三 肺癌蟬聯癌症頭號殺手
- 新聞NEWS一下 / 前總統女婿之弟腦動脈瘤破裂驟逝 「不定時炸彈」 應控制血壓
- 國內猴痘疫情已破百例! 如何減少感染風險?
- 腸病毒71型疫苗上市, 該帶孩子施打嗎?
- 到處都有環境荷爾蒙,危機四伏! 如何減少危害?
- 缺藥風波!換藥可以放心用嗎? ――原廠藥、學名藥釋疑
- 基因檢測 能精準預測疾病,趨吉避凶?(下)
- 小時候胖,不只是胖 兒童及青少年肥胖漸增,埋下慢性病根源!
- 中耳炎頻頻復發,該怎麼辦?
- 心頭小鹿亂撞 ――心悸該擔心嗎?
- 健身族、肌少族熱衷攝取蛋白質! 蛋白質怎麼吃最健康?
- 染燙髮,要注意哪些問題?
- 楊智超醫師專欄 / 發炎性肌肉病變 ―力不從心的無奈
- 消脂保肝專欄 /消脂保肝,自救也救人!
- 曾宇婷醫師專欄 / 監控血糖也要顧眼睛! 小心糖尿病視網膜病變
- 王清泓醫師專欄 / 青光眼如何影響駕車安全?